計算
式量
元素
| 元素 | 式量 [g/mol] |
|---|---|
| \(\rm H\) | \(1\) |
| \(\rm C\) | \(12\) |
| \(\rm N\) | \(14\) |
| \(\rm O\) | \(16\) |
| \(\rm Na\) | \(23\) |
| \(\rm Mg\) | \(24.3^*\) |
| \(\rm Al\) | \(27\) |
| \(\rm S\) | \(32\) |
| \(\rm Cl\) | \(35.5^*\) |
| \(\rm K\) | \(39\) |
| \(\rm Ca\) | \(40\) |
| \(\rm Fe\) | \(56\) |
| \(\rm Zn\) | \(65\) |
| \(\rm Ag\) | \(108\) |
| \(\rm I\) | \(127\) |
| \(\rm Ba\) | \(137\) |
化合物
| 化学式 | 式量 [g/mol] |
|---|---|
| \(\rm C_6H_{12}O_6\) | \(180\) |
| \(\rm C_{12}H_{22}O_{11}\) | \(342\) |
| \(\rm(C_6H_{10}O_5)_{\it n}\) | \(162n\) |
| \(\rm CO_2\) | \(44\) |
| \(\rm HCl\) | \(36.5^*\) |
| \(\rm HNO_3\) | \(63\) |
| \(\rm H_2O\) | \(18\) |
| \(\rm H_2SO_4\) | \(98\) |
| \(\rm NaCl\) | \(58.5^*\) |
| \(\rm NaOH\) | \(40\) |
計算テクニック
| 計算テクニック | 有効桁数 |
|---|---|
| \[22.4=2^5\cdot7\times10^{-1}\approx\frac{20}{9}\] | 2 |
| \[8.31\approx\frac{25}{3}\] | 2 |
分子・結晶
溶液
溶解表
| [\(\rm{}^{\circ}C\)]\[g] | \[\rm H_2O\] | \[\rm S\] |
|---|---|---|
| \[T_0\] | ||
| \[T_1\] |
pH
公式
物質 \(X\) の濃度を \(\bigl[X\bigr]\;\rm[mol/L]\),モル濃度を \(C\;\rm[mol/L]\),体積を \(V\;\rm[L]\),電離度を \(\alpha\;[\text{-}]\),酸・塩基を \(\rm a,\;b\) として,
| \[\begin{align}&\bigl[{\rm H^+}\bigr]=C_{\rm a}V\alpha\\\\ &\bigl[{\rm OH^-}\bigr]=C_{\rm b}V\alpha\end{align}\] |
また,水のイオン積を \(K_{\rm w}\;\rm[mol^2/L^2]\) として,
| \[K_{\rm w}=\bigl[H^+\bigr]\bigl[OH^-\bigr]\approx1.0\times10^{-14}\] |
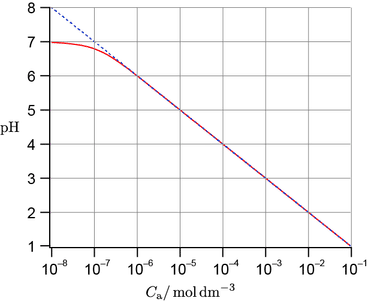
極度に薄い場合
- 強酸
| \[\begin{align}&\begin{cases}&\rm HA_{strong}\rightarrow \underset{{\it C}_{[mol/L]}}{\underline{H^+}} +\underset{{\it C}_{[mol/L]}}{\underline{A_{strong}^-}}\\\\ &\rm H_2O⇄\underset{{\it x}_{[mol/L]}}{\underline{H^+}} +\underset{{\it x}_{[mol/L]}}{\underline{OH^-}}\end{cases}\\\\ \Rightarrow\quad&K_w=(C+x)x\end{align}\] |
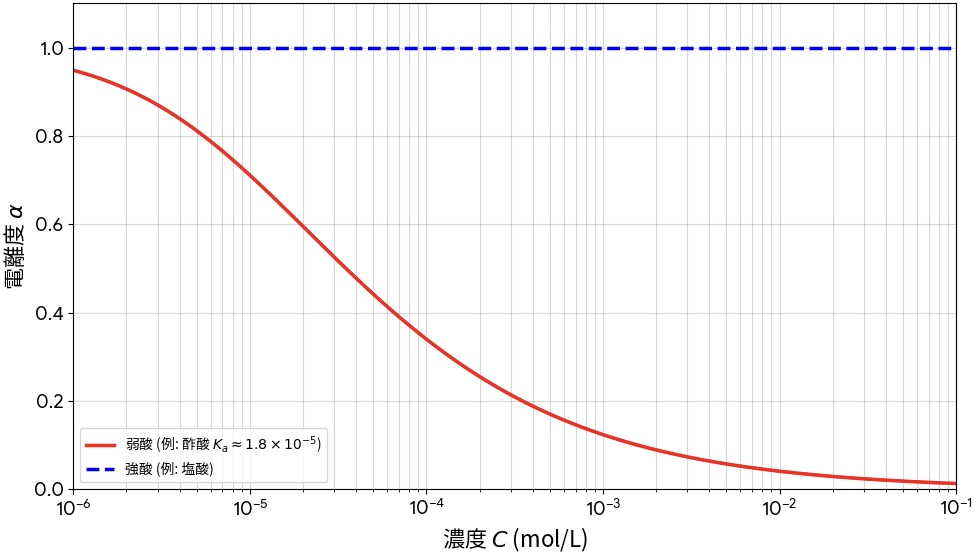
- 弱酸
| \[\begin{align}&\begin{cases}&\rm \underset{{\it C\rm(1-\it\alpha\rm)}_{[mol/L]}}{\underline{HA_{weak}}}⇄ \underset{{\it C\alpha}_{[mol/L]}}{\underline{H^+}} +\underset{{\it C\alpha}_{[mol/L]}}{\underline{A_{weak}^-}}\\\\ &\rm H_2O⇄\underset{{\it x}_{[mol/L]}}{\underline{H^+}} +\underset{{\it x}_{[mol/L]}}{\underline{OH^-}}\end{cases}\\\\ \Rightarrow\quad&K_a=\frac{C\alpha^2}{1-\alpha}\end{align}\] |
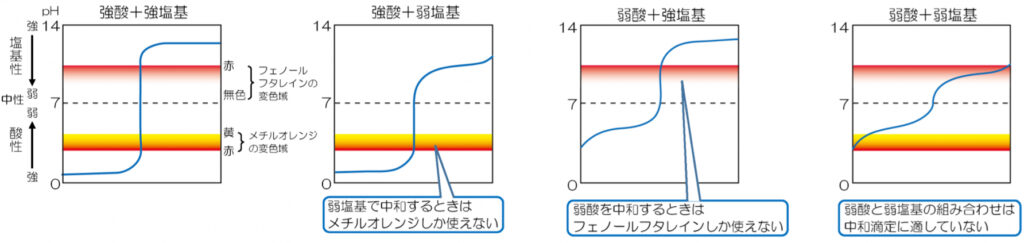
指示薬
上下が入れ替わった場合も然り.
変色域は,
- フェノールフタレイン:\(\rm pH\;8.0\sim9.8\)
- メチルオレンジ:\(\rm pH\;3.1\sim4.4\)
BTB溶液は連続的な変色をするので,中和滴定の指示薬には向いていない.
中和滴定
公式
モル濃度を \(C\;\rm[mol/L]\),体積を \(V\;\rm[L]\),価数を \(k\;\rm[\text{-}]\),酸・塩基を \(\rm a,\;b\) として,
\[
\sum_{\rm a} C_{\rm a} V_{\rm a} k_{\rm a}
=\sum_{\rm b} C_{\rm b} V_{\rm b} k_{\rm b}
\]
または,体積を \(v\;\rm[mL]\) として,
\[
\sum_{\rm a} C_{\rm a} v_{\rm a} k_{\rm a}
=\sum_{\rm b} C_{\rm b} v_{\rm b} k_{\rm b}
\]
操作
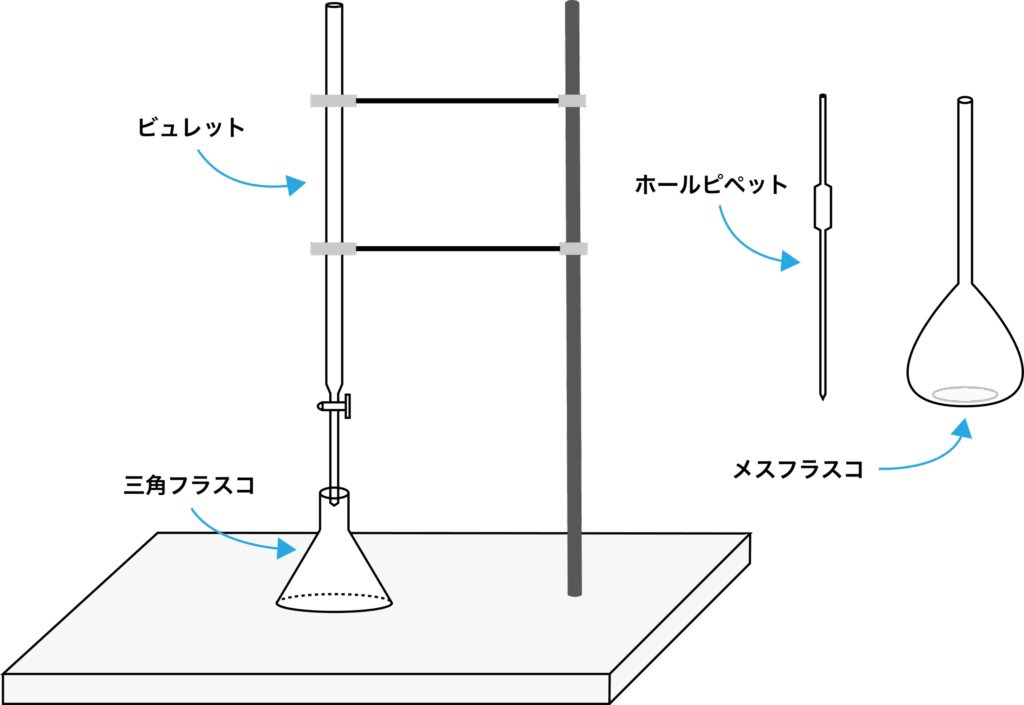
- 標準溶液を「メスフラスコ」で調製する.
- 標準溶液を「ホールピペット」で量り取る.
- 標準溶液を「三角フラスコ」に移す.
- 濃度不明の溶液を「ビュレット」で滴下する.
- 不都合な濃度変化をさせないため,
- ホールピペットとビュレットは共洗いを行う.
- コニカルビーカーは共洗いを行わない.
- 三角フラスコの代わりに「コニカルビーカー」を用いる場合もある.
- ホールピペットは口で吸い上げる場合がある.
- 安全面から「安全ピペッター」を用いる場合がある.
半透膜
ファントホッフの法則
何がどちらへ移動するか図に書く.
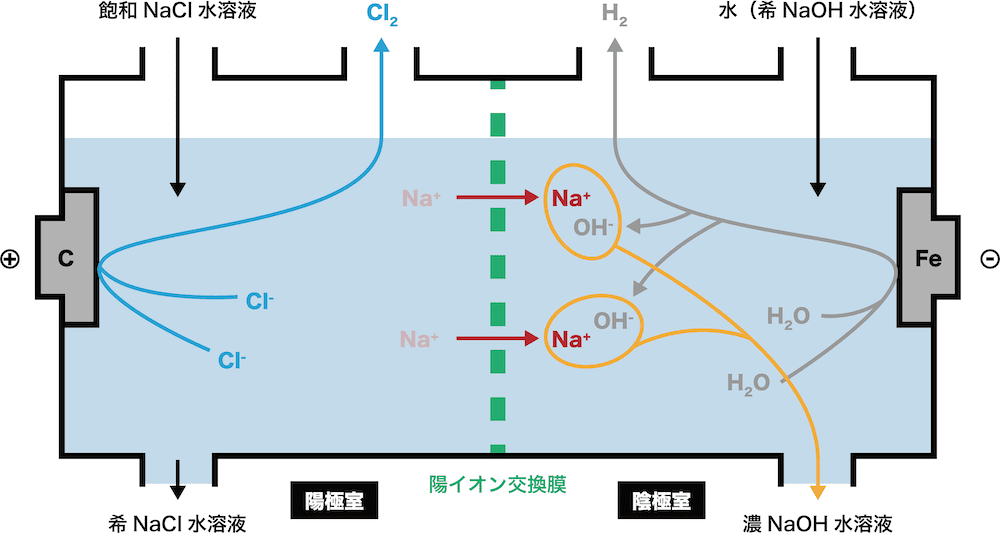
イオン交換膜法
水酸化ナトリウムを濃くし,塩素と水素の単体を取り出す.
ラウールの法則
純溶媒の蒸気圧を \(P_l\),その溶媒のモル分率を \(x_l\) として,蒸気圧 \(P_l’\) は,
| \[P_l’=P_lx_l\] |
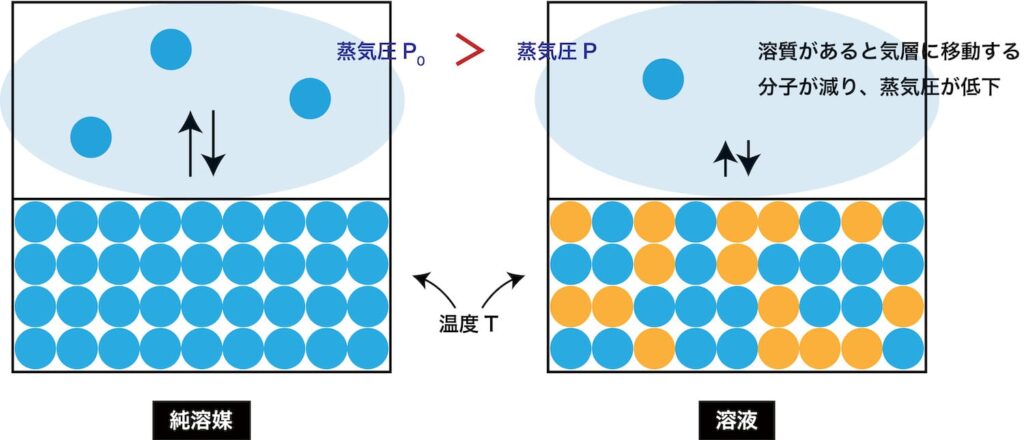
蒸気圧降下
純溶媒時の蒸気圧を \(P_l\),その溶媒の物質量を \(n_l\),電離・会合等を考慮した式量を \(M_l\),溶質の物質量を \(n_s\) として,実際の溶媒の蒸気圧 \(P_l’\) は,
| \[{\it \Delta}P=P_l-P_l’=\frac{n_s}{n_l\color{#bbb}{+n_s}}P_l \approx\underset{モル凝固点降下度\,K}{\underline{P_lM_l\times10^{-3}}}\times \underset{実質質量モル濃度 m}{\underline{\frac{n_s}{n_lM_l\times10^{-3}}}} =Km\] |
気体
基礎方程式
上から,気体の状態方程式,ファントホッフの法則,ヘンリーの法則,ドルトンの法則.
\[\begin{align}
&pV=nRT\\
&{\it\Pi}=CRT=\frac{\rho}{M}RT&&({\it\Pi}V=nRT)\\
&\frac{p}{n}=Const.\\
&\frac{n_1}{n_0}=\frac{p_1}{p_0}&&(p=p_0+p_1)
\end{align}\]
関係する液体がすべて気化した場合,気体の存在比の公式が使える.
気体計算では,バランスシートを書く.
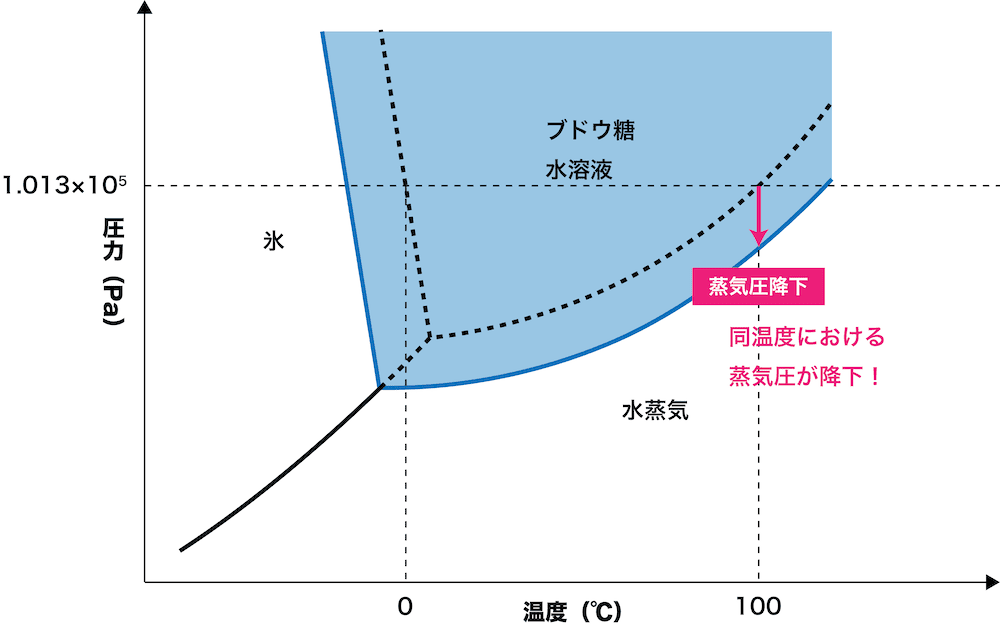
状態図
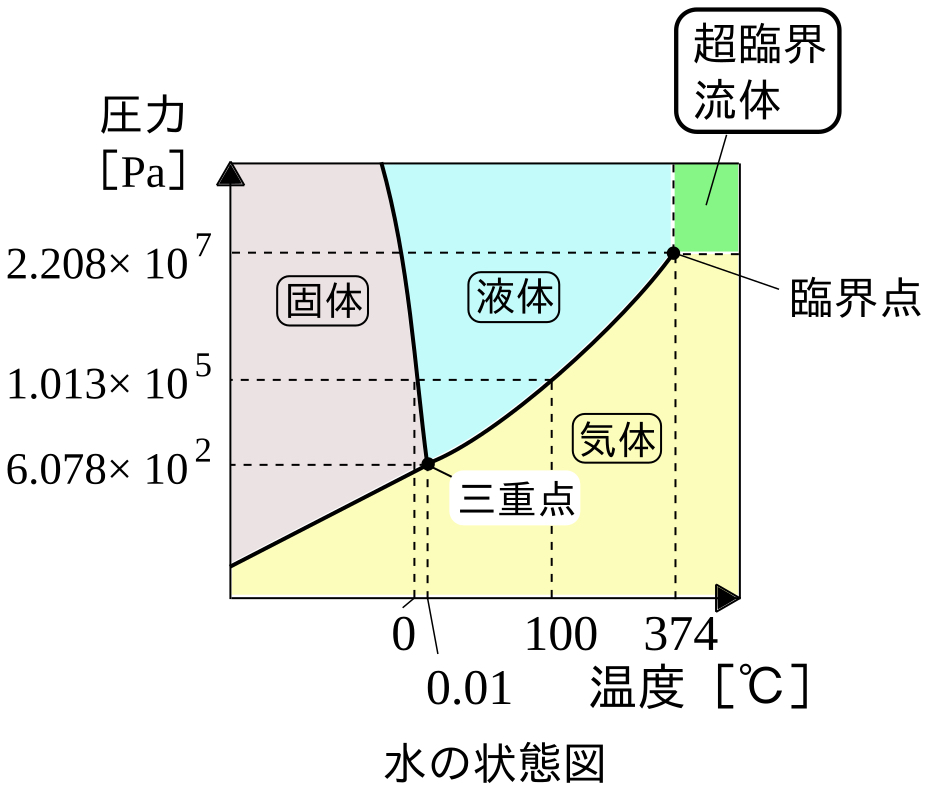
圧力と状態変化
圧力と沸点・昇華点は単調増加,圧力と融点は単調減少の関係にある.
蒸気圧
液体発生の場合,分圧と蒸気圧は等しい.
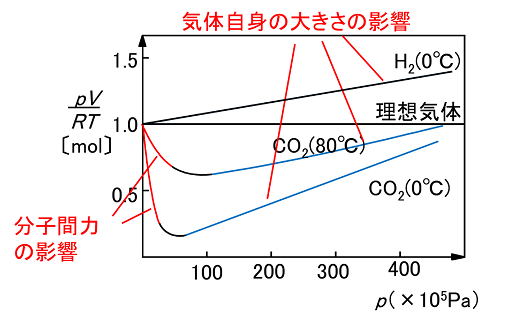
圧縮率因子
低圧ならば分子間力が,高圧ならば体積の影響が大きくなる.
| \[Z=\frac{PV}{nRT}\approx1\] |
酸化還元反応
酸化剤
| 酸化剤 | 生成物 | 半反応式 | 覚え方・ポイント |
|---|---|---|---|
| \(\rm\color{tomato}{MnO_4^-}\) \(\small{(酸性)}\) | \(\rm\color{royalblue}{Mn^{2+}}\) | \(\rm\color{tomato}{MnO_4^-}+8H^++5e^- \rightarrow\rm\color{royalblue}{Mn^{2+}}+4H_2O\) | 赤紫色 → 無色 分解チック |
| \(\rm\color{tomato}{MnO_4^-}\) \(\small{(中・塩)}\) | \(\rm\color{royalblue}{MnO_2}\) | \(\rm\color{tomato}{MnO_4^-}+2H_2O+3e^- \rightarrow\rm\color{royalblue}{MnO_2}+4OH^-\) | 黒色沈殿 中3 |
| \(\rm\color{tomato}{Cr_2O_7^{2-}}\) | \(\rm\color{royalblue}{2Cr^{3+}}\) | \(\rm\color{tomato}{Cr_2O_7^{2-}}+14H^++6e^- \rightarrow\rm\color{royalblue}{2Cr^{3+}}+7H_2O\) | 赤橙色 → 深緑色 分解チック |
| \(\rm\color{tomato}{HNO_3}\) \(\small{(濃)}\) | \(\rm\color{royalblue}{NO_2}\) | \(\rm\color{tomato}{HNO_3}+H^++e^- \rightarrow\rm\color{royalblue}{NO_2}+H_2O\) | 赤褐色気体 濃ければ軽傷 |
| \(\rm\color{tomato}{HNO_3}\) \(\small{(希)}\) | \(\rm\color{royalblue}{NO}\) | \(\rm\color{tomato}{HNO_3}+3H^++3e^- \rightarrow\rm\color{royalblue}{NO}+2H_2O\) | 無色気体 (空気中で赤褐色に) 薄いと酸欠 |
| \(\rm\color{tomato}{H_2SO_4}\) \(\small{(熱濃)}\) | \(\rm\color{royalblue}{SO_2}\) | \(\rm\color{tomato}{H_2SO_4}+2H^++2e^- \xrightarrow{\Delta}\rm \color{royalblue}{SO_2}+2H_2O\) | 刺激臭 |
| \(\rm\color{tomato}{Cl_2}\) | \(\rm\color{royalblue}{2Cl^-}\) | \(\rm\color{tomato}{Cl_2}+2e^- \rightarrow\rm\color{royalblue}{2Cl^-}\) | ハロゲン単体は強酸化剤 酸化力:F\({}_{2}\) > Cl\({}_{2}\) > Br\({}_{2}\) > I\({}_{2}\) |
| \(\rm\color{tomato}{H_2O_2}\) \(\small{(酸性)}\) | \(\rm\color{royalblue}{2H_2O}\) | \(\rm\color{tomato}{H_2O_2}+2H^++2e^- \rightarrow\rm\color{royalblue}{2H_2O}\) | 基本は酸化剤だが, KMnO\({}_{4}\)等に酸化される |
| \(\rm\color{tomato}{SO_2}\) | \(\rm\color{royalblue}{S}\) | \(\rm\color{tomato}{SO_2}+4H^++4e^- \rightarrow\rm\color{royalblue}{S}+2H_2O\) | H\({}_{2}\)S とのときだけ酸化剤 S 生成で白濁 |
| \(\rm\color{tomato}{O_3}\) | \(\rm\color{royalblue}{O_2}\) | \(\rm\color{tomato}{O_3}+2H^++2e^- \rightarrow\rm\color{royalblue}{O_2}+H_2O\) | ヨウ化カリウムデンプン紙を青変 |
還元剤
| 還元剤 | 生成物 | 半反応式 | 覚え方・ポイント |
|---|---|---|---|
| \(\rm\color{royalblue}{(COOH)_2}\) | \(\rm\color{tomato}{2CO_2}\) | \(\rm\color{royalblue}{(COOH)_2} \rightarrow\rm\color{tomato}{2CO_2}+2H^++2e^-\) | 分解チック |
| \(\rm\color{royalblue}{2I^-}\) | \(\rm\color{tomato}{I_2}\) | \(\rm\color{royalblue}{2I^-} \rightarrow\rm\color{tomato}{I_2}+2e^-\) | I\({}_{2}\) 生成で褐色に デンプンで青紫色 |
| \(\rm\color{royalblue}{H_2S}\) | \(\rm\color{tomato}{S}\) | \(\rm\color{royalblue}{H_2S} \rightarrow\rm\color{tomato}{S}+2H^++2e^-\) | S 生成で白濁 腐卵臭 |
| \(\rm\color{royalblue}{SO_2}\) | \(\rm\color{tomato}{SO_4^{2-}}\) | \(\rm\color{royalblue}{SO_2}+2H_2O \rightarrow\rm\color{tomato}{SO_4^{2-}}+4H^++2e^-\) | H\({}_{2}\)S と以外の基本形 \(\rm SO_4^{2-}\) 用の水必須 |
| \(\rm\color{royalblue}{H_2O_2}\) | \(\rm\color{tomato}{O_2}\) | \(\rm\color{royalblue}{H_2O_2} \rightarrow\rm\color{tomato}{O_2}+2H^++2e^-\) | O 発生 |
| \(\rm\color{royalblue}{Sn^{2+}}\) | \(\rm\color{tomato}{Sn^{4+}}\) | \(\rm\color{royalblue}{Sn^{2+}} \rightarrow\rm\color{tomato}{Sn^{4+}}+2e^-\) | Sn は +4 で安定 |
| \(\rm\color{royalblue}{Fe^{2+}}\) | \(\rm\color{tomato}{Fe^{3+}}\) | \(\rm\color{royalblue}{Fe^{2+}} \rightarrow\rm\color{tomato}{Fe^{3+}}+e^-\) | 淡緑色 → 黄褐色 |
| \(\rm\color{royalblue}{Na}\) | \(\rm\color{tomato}{Na^+}\) | \(\rm\color{royalblue}{Na} \rightarrow\rm\color{tomato}{Na^+}+e^-\) | Na, K, Ca, Ba は強力な還元剤 |
| \(\rm\color{royalblue}{2S_2O_3^{2-}}\) | \(\rm\color{tomato}{S_4O_6^{2-}}\) | \(\rm\color{royalblue} {\underset{チオ硫酸ナトリウム}{\underline{2S_2O_3^{2-}}}} \rightarrow\rm\color{tomato}{\underset{四チオン酸イオン} {\underline{S_4O_6^{2-}}}}+2e^-\) | ヨウ素滴定で必須 生成 |
有名酸化還元反応式
| 酸化還元反応式 | 覚え方・ポイント |
|---|---|
| \(\rm\color{tomato}{3Cu}+\color{royalblue}{8HNO_3} \rightarrow\rm\color{royalblue}{3Cu(NO_3)_2}+\color{tomato}{2NO}+4H_2O\) | 三度焼きっしょ、無色だし |
| \(\rm\color{tomato}{Cu}+\color{royalblue}{4HNO_3} \rightarrow\rm\color{royalblue}{Cu(NO_3)_2}+\color{tomato}{2NO_2}+2H_2O\) | 幾代の賞賛、喝采で |
| \(\rm\color{tomato}{Cu}+\color{royalblue}{2H_2SO_4} \xrightarrow{\Delta}\rm\color{royalblue}{CuSO_4}+\color{tomato}{SO_2}+2H_2O\) | 一同に海苔、刺激的 |
| \(\rm\color{tomato}{2MnO_4^-}+\color{royalblue}{5(COOH)_2}+6H^+ \xrightarrow{H_2SO_4}\rm\color{royalblue}{2Mn^{2+}}+\color{tomato}{10CO_2}+8H_2O\) | 普通 |
| \(\rm\color{tomato}{2Na_2S_2O_3}+\color{royalblue}{I_2} \rightarrow\rm\color{royalblue}{Na_2S_4O_6}+\color{tomato}{2NaI}\) | ニッチな一夜、予知にない 沃素澱粉反応の逆 |
| \(\rm\color{tomato}{K_2Cr_2O_7}+\color{royalblue}{3SnCl_2}+14HCl \rightarrow\rm\color{royalblue}{2CrCl_3}+\color{tomato}{3SnCl_4}+2KCl+7H_2O\) | 1 二 3 ス 塩化しろ |
| \(\rm\color{tomato}{SO_2}+\color{royalblue}{2H_2S} \rightarrow\rm\color{royalblue}{3S}+2H_2O\) | 中和チック |
COD(化学的酸素要求量)
試料 1 [L] あたりに含まれる有機物を酸化するために必要な酸素の質量 ([mg]) を求める操作.
操作
- 試料,水,硫酸と硝酸銀水溶液数滴を混ぜる.
- H\({}_{2}\)SO\({}_{4}\): 酸性環境 (Mn\({}^{2+}\)化) を整え,酸化還元に無影響.
- AgNO\({}_{3}\): 試料中の還元剤である塩素を沈殿.
- 過剰な過マンガン酸カリウムを加えて 30 分間加熱.
- KMnO\({}_{4}\): 酸化剤と指示薬を両立し,そこそこ安全.
- 過剰のシュウ酸ナトリウムを加えてクエンチ.
- (COONa)\({}_{2}\): 純度が高く安定で無色.
- 過マンガン酸カリウムで滴定を行う.
- R(有機物+蓚酸) vs. O(過マンガン酸カリウム)
反応式
君が2人で蓚さん5人,透明感はそのままに.
| \[\rm\color{tomato}{2KMnO_4}+\color{royalblue}{5(COONa)_2}+8H_2SO_4 \rightarrow\rm\color{royalblue}{2MnSO_4}+K_2SO_4+5Na_2SO_4 +\color{tomato}{10CO_2}+8H_2O\] |
電池
1 つの電子が \(n\)個分の活物質を通るので,電池を \(n\) 個直列接続すると,単位電子あたりに消費される活物質は \(n\) 倍
エンタルピー・エントロピー
主要エンタルピー
| 種類 | 補足 |
|---|---|
| 中和エンタルピー | \({\it\Delta}H=-55.8\) |
熱の発生
\(n\;\rm[mol]\) ある物質の \(1\;\rm[mol]\) の反応エンタルピーを \({\it \Delta} H\;\rm[kJ/mol]\),反応後の周辺の物体の比熱を \(c\;\rm[J/(g\cdot K)]\),質量を \(m\;\rm[g]\) ,温度変化を \(T\;\rm[K]\)として,
\[
n{\it \Delta}H=-cm{\it \Delta}T\times\frac{1}{1000}
\]
平衡
温度一定 \(\Rightarrow\) 平衡定数一定.
これを実現するためにルシャトリエの原理がある.
緩衝液
酸には \(CH_3COO^-\) を,塩基には \(CH_3COOH\) をすべて使う.
| \[\begin{align}\rm CH_3COOH⇄H^++CH_3COO^-\\\\ &K_a=\rm\frac{[H^+][CH_3COO^-]}{[CH_3COOH]} \approx2.8\times10^{-5}[mol/L]\end{align}\] |
反応速度
濃度 \(C\),温度,触媒,表面積に依存.
触媒は活性化エネルギーを小さくするが,エンタルピーは変化させない.
反応速度定数 \(k\) は主反応に左右されるため,実験算出.
| \[v=k\frac{dC}{dt}\;(>0)\] |
主な触媒
- 不均一触媒:反応物と状態が異なるもの
| 触媒 | 用例 |
|---|---|
| 酸化マンガン(Ⅳ) | 過酸化水素水の分解 |