分野




酸・塩基
アレニウスの定義
\[\begin{align}
&酸&&\rightarrow&&\rm H^+\;を放出\\\\
&アルカリ&&\rightarrow&&\rm OH^-\;を放出
\end{align}\]
ブリンステッド・ローリーの定義
\[\begin{align}
&酸&&\rightarrow&&プロトン供与体\\\\
&塩基&&\rightarrow&&プロトン受容体
\end{align}\]
ルイスの定義
\[\begin{align}
&酸&&\rightarrow&&電子対受容体\\\\
&塩基&&\rightarrow&&電子対供与体
\end{align}\]
オキソ酸の傾向
Oが多いほど,次点で中心元素の電気陰性度が大きいほど強酸になる傾向にある.
酸化剤・還元剤
酸化剤
| 酸化剤 | 生成物 | 半反応式 | 覚え方・ポイント |
|---|---|---|---|
| \(\rm\color{tomato}{MnO_4^-}\) \(\small{(酸性)}\) | \(\rm\color{royalblue}{Mn^{2+}}\) | \(\rm\color{tomato}{MnO_4^-}+8H^++5e^- \rightarrow\rm\color{royalblue}{Mn^{2+}}+4H_2O\) | 赤紫色 → 無色 分解チック |
| \(\rm\color{tomato}{MnO_4^-}\) \(\small{(中・塩)}\) | \(\rm\color{royalblue}{MnO_2}\) | \(\rm\color{tomato}{MnO_4^-}+2H_2O+3e^- \rightarrow\rm\color{royalblue}{MnO_2}+4OH^-\) | 黒色沈殿 中3 |
| \(\rm\color{tomato}{Cr_2O_7^{2-}}\) | \(\rm\color{royalblue}{2Cr^{3+}}\) | \(\rm\color{tomato}{Cr_2O_7^{2-}}+14H^++6e^- \rightarrow\rm\color{royalblue}{2Cr^{3+}}+7H_2O\) | 赤橙色 → 深緑色 分解チック |
| \(\rm\color{tomato}{HNO_3}\) \(\small{(濃)}\) | \(\rm\color{royalblue}{NO_2}\) | \(\rm\color{tomato}{HNO_3}+H^++e^- \rightarrow\rm\color{royalblue}{NO_2}+H_2O\) | 赤褐色気体 濃ければ軽傷 |
| \(\rm\color{tomato}{HNO_3}\) \(\small{(希)}\) | \(\rm\color{royalblue}{NO}\) | \(\rm\color{tomato}{HNO_3}+3H^++3e^- \rightarrow\rm\color{royalblue}{NO}+2H_2O\) | 無色気体 (空気中で赤褐色に) 薄いと酸欠 |
| \(\rm\color{tomato}{H_2SO_4}\) \(\small{(熱濃)}\) | \(\rm\color{royalblue}{SO_2}\) | \(\rm\color{tomato}{H_2SO_4}+2H^++2e^- \xrightarrow{\it Delta}\rm \color{royalblue}{SO_2}+2H_2O\) | 刺激臭 |
| \(\rm\color{tomato}{Cl_2}\) | \(\rm\color{royalblue}{2Cl^-}\) | \(\rm\color{tomato}{Cl_2}+2e^- \rightarrow\rm\color{royalblue}{2Cl^-}\) | ハロゲン単体は強酸化剤 酸化力:F\({}_{2}\) > Cl\({}_{2}\) > Br\({}_{2}\) > I\({}_{2}\) |
| \(\rm\color{tomato}{H_2O_2}\) \(\small{(酸性)}\) | \(\rm\color{royalblue}{2H_2O}\) | \(\rm\color{tomato}{H_2O_2}+2H^++2e^- \rightarrow\rm\color{royalblue}{2H_2O}\) | 基本は酸化剤だが, KMnO\({}_{4}\)等に酸化される |
| \(\rm\color{tomato}{SO_2}\) | \(\rm\color{royalblue}{S}\) | \(\rm\color{tomato}{SO_2}+4H^++4e^- \rightarrow\rm\color{royalblue}{S}+2H_2O\) | H\({}_{2}\)S とのときだけ酸化剤 S 生成で白濁 |
| \(\rm\color{tomato}{O_3}\) | \(\rm\color{royalblue}{O_2}\) | \(\rm\color{tomato}{O_3}+2H^++2e^- \rightarrow\rm\color{royalblue}{O_2}+H_2O\) | ヨウ化カリウムデンプン紙を青変 |
還元剤
| 還元剤 | 生成物 | 半反応式 | 覚え方・ポイント |
|---|---|---|---|
| \(\rm\color{royalblue}{(COOH)_2}\) | \(\rm\color{tomato}{2CO_2}\) | \(\rm\color{royalblue}{(COOH)_2} \rightarrow\rm\color{tomato}{2CO_2}+2H^++2e^-\) | 分解チック |
| \(\rm\color{royalblue}{2I^-}\) | \(\rm\color{tomato}{I_2}\) | \(\rm\color{royalblue}{2I^-} \rightarrow\rm\color{tomato}{I_2}+2e^-\) | I\({}_{2}\) 生成で褐色に デンプンで青紫色 |
| \(\rm\color{royalblue}{H_2S}\) | \(\rm\color{tomato}{S}\) | \(\rm\color{royalblue}{H_2S} \rightarrow\rm\color{tomato}{S}+2H^++2e^-\) | S 生成で白濁 腐卵臭 |
| \(\rm\color{royalblue}{SO_2}\) | \(\rm\color{tomato}{SO_4^{2-}}\) | \(\rm\color{royalblue}{SO_2}+2H_2O \rightarrow\rm\color{tomato}{SO_4^{2-}}+4H^++2e^-\) | H\({}_{2}\)S と以外の基本形 \(\rm SO_4^{2-}\) 用の水必須 |
| \(\rm\color{royalblue}{H_2O_2}\) | \(\rm\color{tomato}{O_2}\) | \(\rm\color{royalblue}{H_2O_2} \rightarrow\rm\color{tomato}{O_2}+2H^++2e^-\) | O 発生 |
| \(\rm\color{royalblue}{Sn^{2+}}\) | \(\rm\color{tomato}{Sn^{4+}}\) | \(\rm\color{royalblue}{Sn^{2+}} \rightarrow\rm\color{tomato}{Sn^{4+}}+2e^-\) | Sn は +4 で安定 |
| \(\rm\color{royalblue}{Fe^{2+}}\) | \(\rm\color{tomato}{Fe^{3+}}\) | \(\rm\color{royalblue}{Fe^{2+}} \rightarrow\rm\color{tomato}{Fe^{3+}}+e^-\) | 淡緑色 → 黄褐色 |
| \(\rm\color{royalblue}{Na}\) | \(\rm\color{tomato}{Na^+}\) | \(\rm\color{royalblue}{Na} \rightarrow\rm\color{tomato}{Na^+}+e^-\) | Na, K, Ca, Ba は強力な還元剤 |
| \(\rm\color{royalblue}{2S_2O_3^{2-}}\) | \(\rm\color{tomato}{S_4O_6^{2-}}\) | \(\rm\color{royalblue} {\underset{チオ硫酸ナトリウム}{\underline{2S_2O_3^{2-}}}} \rightarrow\rm\color{tomato}{\underset{四チオン酸イオン} {\underline{S_4O_6^{2-}}}}+2e^-\) | ヨウ素滴定で必須 生成 |
有名酸化還元反応式
| 酸化還元反応式 | 覚え方・ポイント |
|---|---|
| \(\rm\color{tomato}{3Cu}+\color{royalblue}{8HNO_3} \rightarrow\rm\color{royalblue}{3Cu(NO_3)_2}+\color{tomato}{2NO}+4H_2O\) | 三度焼きっしょ、無色だし |
| \(\rm\color{tomato}{Cu}+\color{royalblue}{4HNO_3} \rightarrow\rm\color{royalblue}{Cu(NO_3)_2}+\color{tomato}{2NO_2}+2H_2O\) | 幾代の賞賛、喝采で |
| \(\rm\color{tomato}{Cu}+\color{royalblue}{2H_2SO_4} \xrightarrow{\it \Delta}\rm\color{royalblue}{CuSO_4}+\color{tomato}{SO_2}+2H_2O\) | 一同に海苔、刺激的 |
| \(\rm\color{tomato}{2MnO_4^-}+\color{royalblue}{5(COOH)_2}+6H^+ \xrightarrow{H_2SO_4}\rm\color{royalblue}{2Mn^{2+}}+\color{tomato}{10CO_2}+8H_2O\) | 普通 |
| \(\rm\color{tomato}{2Na_2S_2O_3}+\color{royalblue}{I_2} \rightarrow\rm\color{royalblue}{Na_2S_4O_6}+\color{tomato}{2NaI}\) | ニッチな一夜、予知にない 沃素澱粉反応の逆 |
| \(\rm\color{tomato}{K_2Cr_2O_7}+\color{royalblue}{3SnCl_2}+14HCl \rightarrow\rm\color{royalblue}{2CrCl_3}+\color{tomato}{3SnCl_4}+2KCl+7H_2O\) | 1 二 3 ス 塩化しろ |
| \(\rm\color{tomato}{SO_2}+\color{royalblue}{2H_2S} \rightarrow\rm\color{royalblue}{3S}+2H_2O\) | 中和チック |
化学薬品の保存・取り扱い注意点まとめ
| 推奨 | 理由 | 主対象物質 | 覚え方・ポイント |
|---|---|---|---|
| 褐色びん | 光分解性 | \(HNO_3\) aq \(AgNO_3\) aq \(H_2O_2\) aq \(Cl_2\) aq Br\({}_{2}\) (\(l\)) KI | 1 電子の授受で変化しやすい |
| ポリ容器 | ガラス溶解性 | \(HF\) | \(\rm SiO_2+6HF\rightarrow \underset{ヘキサフルオロケイ酸}{\underline{H_2SiF_6}} +2H_2O\) |
| ガラス栓 | ゴム溶解性 ゴム腐食性 | 有機溶媒 酸化力の強い液体 | 有機物 × 有機溶媒 シス体を台無しにする |
| ゴム栓 | ガラスの固着 | 強塩基の水溶液 | ソーダ石灰ガラス: SiO\({}_{2}\)-Na–\({}_{2}\)O-CaO |
| 石油中 | 酸素・水反応性 | アルカリ金属 | Li は石油に浮くので、パラフィン等で覆う |
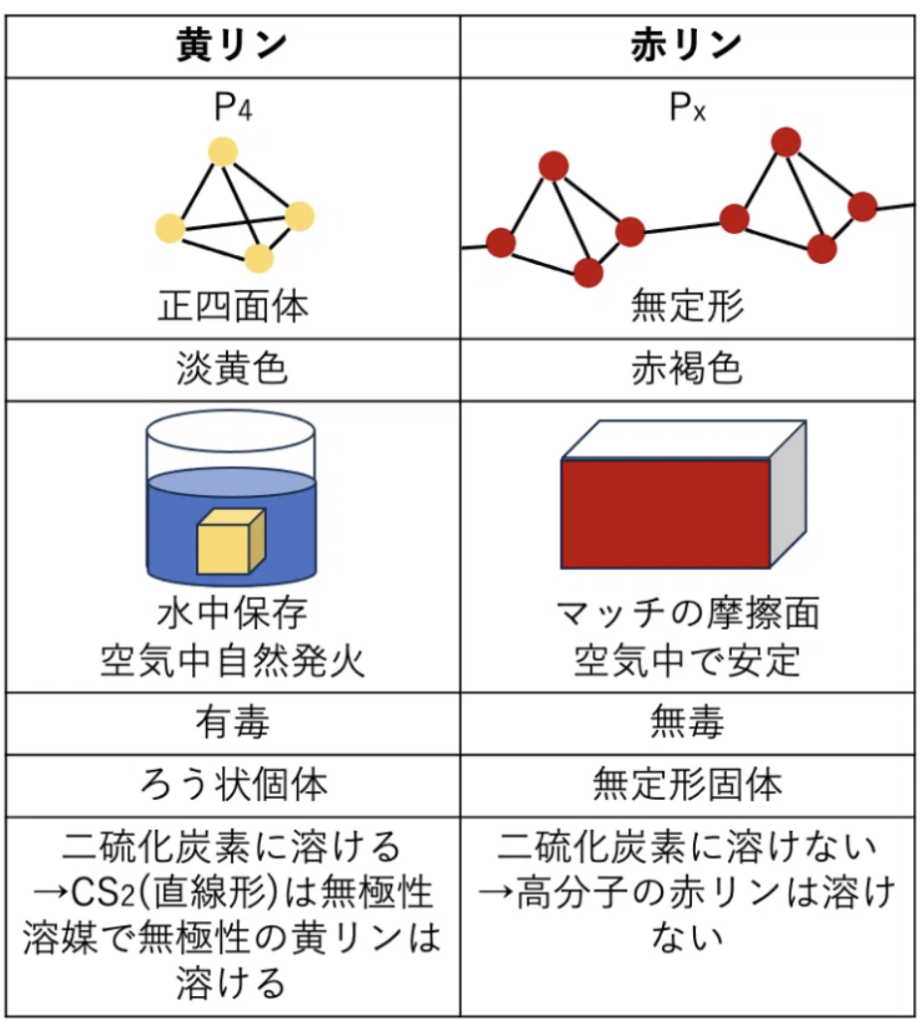
| 水中 | 空気中で自然発火 | 黄リン (\(P_4\)) | 毒舌キリン、脱水で炎上 |
| 避乾燥剤 \(CaCl_2\) | 付加化合物生成 | \(NH_3\) | \(\rm CaCl_2+8NH_3 \rightarrow \underline{CaCl_2 \cdot 8NH_3}\) |
| 避乾燥剤 (濃硫酸) | 中和・酸化 | \(NH_3\) (塩基) \(H_2S\) (還元) | 酸性乾燥剤 × 塩基性ガス 酸化剤(\(H_2SO_4\)) × 還元剤(\(H_2S\)) |
| 密閉保存 | 潮解・風解 | \(NaOH\) (潮解) \(Na_2CO_3 \cdot 10H_2O\) (風解) \(\rm HCl\) (揮発) | 物質の変質や容器の破裂を防ぐ |
融沸点
原則,ファンデルワールス力 < 水素結合 < 金属結合 < 共有結合.
| 物質(沸点昇順) | 液体温度 \([\rm{}^\circ C]\) |
|---|---|
| \[\rm NH_3\] | \[-33.3\sim-77.7\] |
| \[\rm HF\] | \[-83.6\sim19.5\] |
| \[\rm H_2O\] | \[0\sim100\] |
| \[\rm Ga\] | \[30\sim2400\] |
| \[\rm W\] | \[3400\sim5555\] |
においのある気体
| におい | 物質名 |
|---|---|
| 刺激臭 | \[\rm NH_3,\;SO_2\] |
| 特異臭 | \[\rm O_3\] |
| 腐卵臭 | \[\rm H_2S\] |
周期律

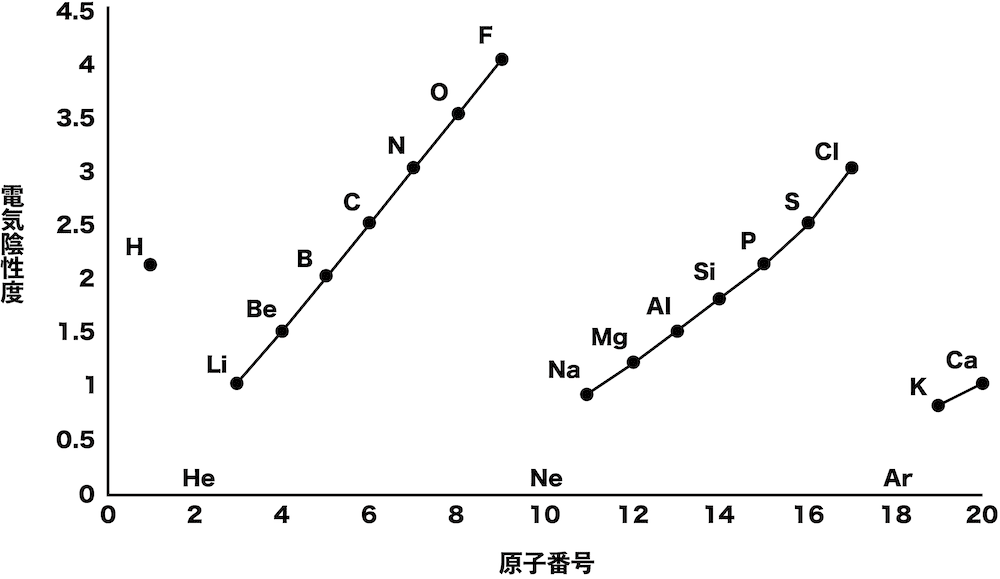
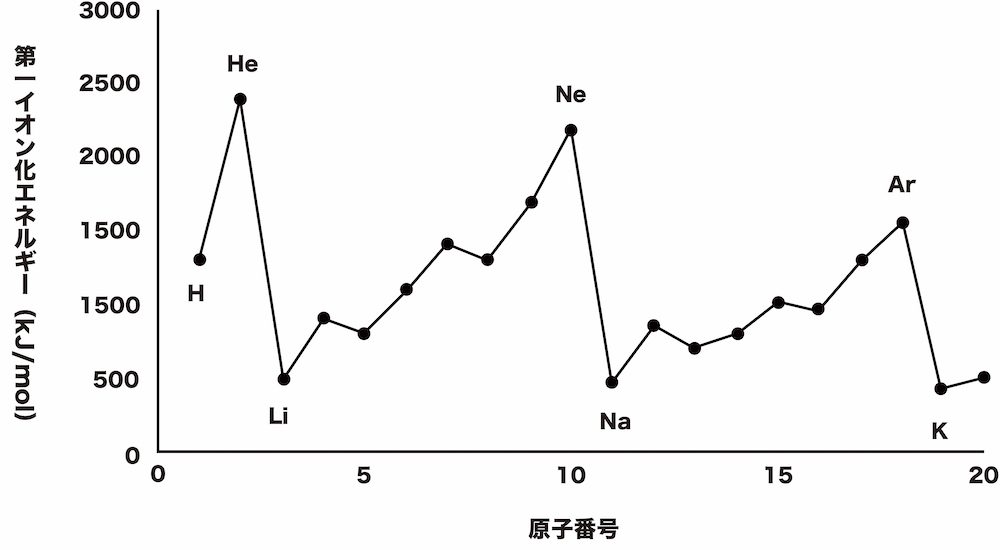
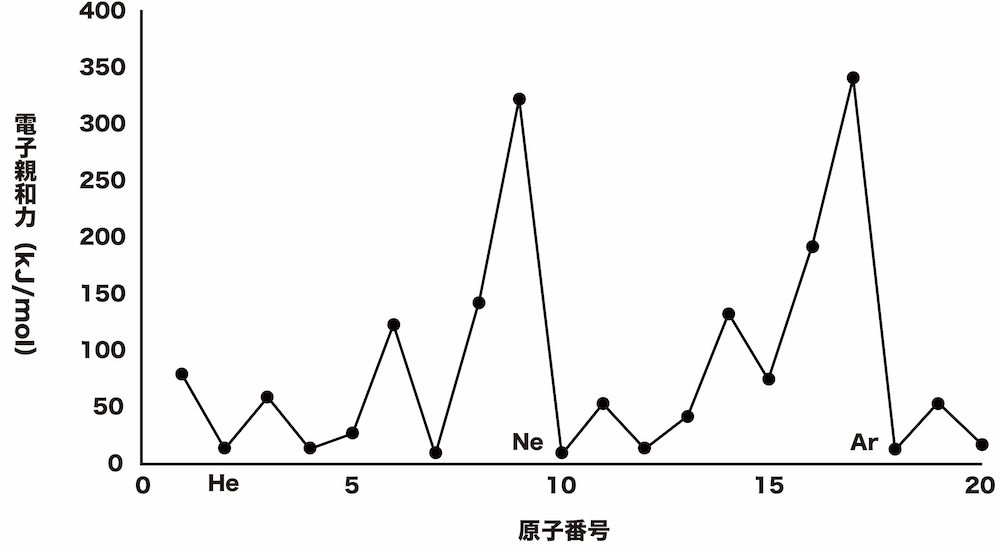
電子配置
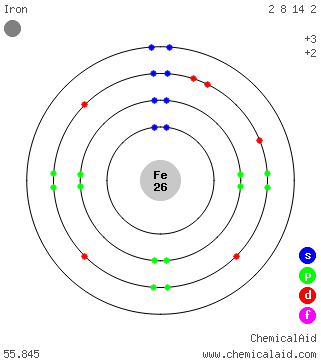
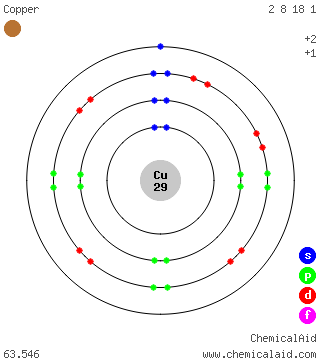
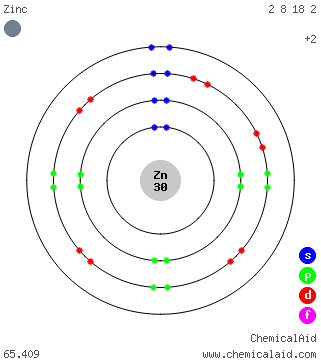
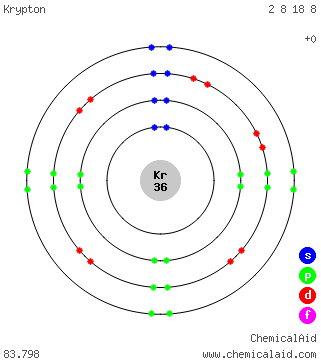
主な無機物
リン
金属イオンの分離と確認
純粋な色
| \[化学式(有色)\] |
|---|
| \[\begin{align} &\rm\color{blue}{Cu^{2+}} \;(青)\\ &\rm\color{lightgreen}{Fe^{2+}} \;(淡緑)\\ &\rm\color{yellow}{Fe^{3+}} \;(黄褐)\\ &\rm\color{green}{Ni^{2+}} \;(緑)\\ &\rm\color{pink}{Mn^{2+}} \;(淡桃)\\ &\rm\color{darkgreen}{Cr^{3+}} \;(暗緑)\\ &\rm\color{yellow}{CrO_4^{2-}} \;(黄)\\ &\rm\color{orangered}{Cr_2O_7^{2-}} \;(赤橙)\\ &\rm\color{violet}{MnO_4^-} \;(赤紫)\\ &\rm\color{darkgreen}{MnO_4^{2-}} \;(暗緑)\\ &\rm\color{brown}{I^{3-}} \;(褐) \end{align}\] |
苛性ソーダ
| \[状態\] | \[\rm NaOH\;(少量)\] | \[\rm NaOH\;(多量)\] | \[加熱\] |
|---|---|---|---|
| \[ 沈殿 (固体) \] | \[\begin{align} &\rm\color{lightgray}{Al(OH)_3} \;(白)\\ &\rm\color{lightgray}{Mn(OH)_2} \;(白)\\ &\rm\color{lightgray}{Zn(OH)_2} \;(白)\\ &\rm\color{#5B8063} {Cr(OH)_3} \;(灰緑)\\ &\rm\color{lightgreen} {Fe(OH)_2} \;(緑白)\\ &\rm\color{green} {Ni(OH)_2} \;(緑)\\ &\rm\color{lightgray}{Sn(OH)_2} \;(白)\\ &\rm\color{lightgray}{Pb(OH)_2} \;(白)\\ &\rm\color{skyblue}{Cu(OH)_2} \;(青白)\\\\ &\rm\color{brown} {MnO(OH)} \;(褐)\\ &\rm\color{darkred} {水酸化鉄(I\!I\!I)} \;(赤褐)\\\\ &\rm\color{yellow}{HgO} \;(黄)\\ &\rm\color{#81805E}{Ag_2O} \;(暗褐) \end{align}\] | \[\begin{align} &\rm\color{lightgray}{Mn(OH)_2} \;(白)\\ &\rm\color{#5B8063} {Cr(OH)_3} \;(灰緑)\\ &\rm\color{lightgreen} {Fe(OH)_2} \;(緑白)\\ &\rm\color{green} {Ni(OH)_2} \;(緑)\\ &\rm\color{skyblue}{Cu(OH)_2} \;(青白)\\\\ &\rm\color{brown} {MnO(OH)} \;(褐)\\ &\rm\color{darkred} {水酸化鉄(I\!I\!I)} \;(赤褐)\\\\ &\rm\color{yellow}{HgO} \;(黄)\\ &\rm\color{#81805E}{Ag_2O} \;(暗褐) \end{align}\] | \[\begin{align} &\rm\color{#5B8063} {MnO} \;(灰緑)\\ &\rm\color{darkgreen} {Cr_2O_3} \;(暗緑)\\ &\rm\color{black} {FeO} \;(黒)\\ &\rm\color{green} {NiO} \;(緑)\\ &\rm\color{black} {CuO} \;(黒)\\\\ &\rm\color{#654321} {Mn_2O_3} \;(黒褐)\\ &\rm\color{darkred} {Fe_2O_3} \;(赤褐)\\\\ &\rm\color{yellow} {HgO} \;(黄)\\ &\rm\color{#81805E}{Ag_2O} \;(暗褐) \end{align}\] |
| \[ 錯イオン \] | – | \[\begin{align} &\rm[Al(OH)_4]^- \;(無,正方)\\ &{}^*\rm[Mn(OH)_4]^{2-} \;(無,正方)\\ &\rm[Sn(OH)_6]^{2-} \;(無,正八面)\\ &\rm[Pb(OH)_4]^{2-} \;(無,正四面)&& \end{align}\] | \[\begin{align} &\rm\color{lightgray} {Al_2O_3} \;(無\cdot 白)\\ &\rm\color{lightgray} {ZnO} \;(白)\\ &\rm\color{gray} {SnO} \;(黒灰)\\ &\rm\color{gold} {PbO} \;(黄〜赤)&& \end{align}\] |
アンモニア
| \[ 状態 \] | \[\rm NH_3\;(少量) \] | \[\rm NH_3\;(多量) \] |
|---|---|---|
| \[ 沈殿 \] | \[\begin{align} &\rm\color{lightgray}{Al(OH)_3} \;(白)\\ &\rm\color{lightgray}{Sn(OH)_2} \;(白)\\ &\rm\color{lightgray}{Pb(OH)_2} \;(白)\\ &\rm\color{lightgreen} {Fe(OH)_2} \;(緑白)\\ &\rm\color{darkred} {水酸化鉄(I\!I\!I)} \;(赤褐)\\\\ &\rm\color{#81805E} {Ag_2O} \;(暗褐)\\ &\rm\color{lightgray}{Zn(OH)_2} \;(白)\\ &\rm\color{skyblue} {Cu(OH)_2} \;(青白) \end{align}\] | \[\begin{align} &\rm\color{lightgray}{Al(OH)_3} \;(白)\\ &\rm\color{lightgray}{Sn(OH)_2} \;(白)\\ &\rm\color{lightgray}{Pb(OH)_2} \;(白)\\ &\rm\color{lightgreen} {Fe(OH)_2} \;(緑白)\\ &\rm\color{darkred} {水酸化鉄(I\!I\!I)} \;(赤褐) \end{align}\] |
| \[ 錯イオン \] | – | \[\begin{align} &\rm[Ag(NH_3)_4]^+ \;(無,直線)\\ &\rm[Zn(NH_3)_4]^{2+} \;(無,正四面)\\ &\rm\color{blue} {[Cu(NH_3)_4]^{2+}} \;(深青,正方)\\ &\rm{}^*\color{orange} {[Co(NH_3)_6]^{3+}} \;(橙,正八面)\\ &\rm{}^*\color{blueviolet} {[Ni(NH_3)_6]^{2+}} \;(青紫,正八面)&& \end{align}\] |
青酸カリ
| \[ 状態 \] | \[\rm KCN\;(多量) \] |
|---|---|
| \[ 沈殿 \] | – |
| \[ 錯イオン \] | \[\begin{align} &\rm[Ag(CN)_2]^- \;(無)\\ &\rm[Zn(CN)_4]^{2-} \;(無)\\ &\rm\color{gold} {[Fe(CN)_6]^{3-}} \;(黄褐)\\ &\rm\color{khaki} {[Fe(CN)_6]^{4-}} \;(淡黄)&&\\ \end{align}\] |
酸化物
| \[+1\] | \[+2\] | \[ +2,+3 \] | \[+3\] | \[+4\] | \[+7\] | |
|---|---|---|---|---|---|---|
| \[\rm Mg\] | \[ \rm\color {lightgray} {MgO} \;(白) \] | |||||
| \[\rm Al\] | \[ \rm\color {lightgray} {Al_2O_3} \;(無\cdot 白) \] | |||||
| \[\rm Mn\] | \[ \rm\color {#5B8063} {MnO} \;(灰緑) \] | \[ \rm\color {darkred} {Mn_3O_4} \;(赤褐) \] | \[ \rm\color {#654321} {Mn_2O_3} \;(黒褐) \] | \[ \rm\color {#604020} {MnO_2} \;(黒褐) \] | \[ \rm\color {darkgreen} {Mn_2O_7} \;(暗緑) \] | |
| \[\rm Zn\] | \[ \rm\color {lightgray} {ZnO} \;(白) \] | |||||
| \[\rm Cr\] | \[ \rm\color {darkgreen} {Cr_2O_3} \;(暗緑) \] | |||||
| \[\rm Fe\] | \[ \rm\color {black} {FeO} \;(黒) \] | \[ \rm\color {black} {Fe_3O_4} \;(黒) \] | \[ \rm\color {darkred} {Fe_2O_3} \;(赤褐) \] | |||
| \[\rm Ni\] | \[ \rm\color {green} {NiO} \;(緑) \] | |||||
| \[\rm Sn\] | \[ \rm\color {gray} {SnO} \;(黒灰) \] | \[ \rm\color {lightgray} {SnO_2} \;(白灰) \] | ||||
| \[\rm Pb\] | \[ \rm\color {gold} {PbO} \;(黄〜赤) \] | \[ \rm\color {red} {Pb_3O_4} \;(赤) \] | \[ \rm\color {#654321} {PbO_2} \;(黒褐) \] | |||
| \[\rm Cu\] | \[ \rm\color {red} {Cu_2O} \;(赤) \] | \[ \rm\color {black} {CuO} \;(黒) \] | ||||
| \[\rm Hg\] | \[ \rm\color {yellow} {HgO} \;(黄) \] | |||||
| \[\rm Ag\] | \[ \rm\color {#81805E} {Ag_2O} \;(暗褐) \] |
硫化水素
| \[ 反応前 \] | \[ 沈殿 \] | |
|---|---|---|
| \[ 中,塩基性 \] | \[\begin{align} &\rm\color{} {Al^{3+}} \;(無)\\ &\rm\color{lightpink} {Mn^{2+}} \;(淡赤)&&\\ &\rm\color{} {Zn^{2+}} \;(無)\\ &\rm\color{lightgreen} {Fe^{2+}} \;(淡緑)\\ &\rm\color{gold} {Fe^{3+}} \;(黄褐)\\ &\rm\color{green} {Ni^{2+}} \;(緑)\\ \end{align}\] | \[\begin{align} &\rm\color{lightgray} {Al(OH)_3} \;(白)\\ &\rm\color{pink} {MnS} \;(淡桃)\\ &\rm\color{lightgray} {ZnS} \;(白)\\ &\rm\color{black} {FeS} \;(黒)\\ &\rm\color{black} {FeS} \;(黒)\\ &\rm\color{black} {NiS} \;(黒)\\ \end{align}\] |
| \[ 酸性 \] | \[\begin{align} &\rm\color{gold} {Fe^{3+}} \;(黄褐)\\ \end{align}\] | \[\begin{align} &\rm\color{lightgreen} {Fe^{2+}} \;(淡緑)\\ \end{align}\] |
| \[ 強酸性 \] | \[\begin{align} &\rm\color{} {Cd^{2+}} \;(無)\\ \end{align}\] | \[\begin{align} &\rm\color{yellow} {CdS} \;(黄)\\ \end{align}\] |
| \[ いつでも \] | \[\begin{align} &\rm\color{} {Sn^{2+}} \;(無)\\ &\rm\color{} {Pb^{2+}} \;(無)\\ &\rm\color{blue} {Cu^{2+}} \;(青)\\ &\rm\color{} {Hg^{2+}} \;(無)\\ &\rm\color{} {Ag^+} \;(無)\\ \end{align}\] | \[\begin{align} &\rm\color{blown} {SnS} \;(褐)\\ &\rm\color{black} {PbS} \;(黒)\\ &\rm\color{black} {CuS} \;(黒)\\ &\rm\color{black} {HgS} \;(黒)\\ &\rm\color{black} {Ag_2S} \;(黒)\\ \end{align}\] |
主なハロゲン化金属の色と水への溶解
| \[\rm F \] | \[\rm Cl \] | \[\rm Br \] | \[\rm I \] | |
|---|---|---|---|---|
| \[\rm Fe \] | \[\begin{align} &\rm\color {green} {FeF_3(s)} \;(緑)\\ &\rm\color {pink} {FeF_3\cdot 3H_2O \downarrow} \;(淡桃)\; \end{align}\] | \[\begin{align} &\rm\color {gold} {FeCl_3(s)} \;(黄褐)\\ &\rm\color {darkred} {FeCl_3\,aq} \;(赤褐) \end{align}\] | \[\begin{align} &\rm\color {darkred} {FeCl_3(s)} \;(赤褐)\\ &\rm\color {darkgreen} {FeBr_3\,aq} \;(暗緑)\; \end{align}\] | |
| \[\rm Pb \] | \[\rm \color{lightgray} {PbF_2 \downarrow} \;(白) \] | \[\begin{align} &\quad\;\;\; \rm\color{lightgray} {PbCl_2 \downarrow} \;(白)\\ &\xrightarrow{\Delta} \;\rm\color{} {PbCl_2\,aq} \;(無) \end{align}\] | \[\rm \color{lightgray} {PbBr_2 \downarrow} \;(白) \] | \[\rm \color{yellow} {PbI_2} \;(黄) \] |
| \[\rm Ag \] | \[\begin{align} &\rm\color {yellow} {AgF(s)} \;(黄)\\ &\rm\color{} {AgF\,aq} \;(無) \end{align}\] | \[\begin{align} &\rm\color{lightgray} {AgCl \downarrow} \;(白)\\ &\rm\color{lightgray} {Ag_2Cl_2 \downarrow} \;(白) \end{align}\] | \[\rm \color {khaki} {AgBr \downarrow} \;(淡黄) \] | \[\rm \color{yellow} {AgI \downarrow} \;(黄) \] |
| \[\rm Hg \] | \[\begin{align} &\rm\color {yellow} {HgF(s)} \;(黄)\\ &\rm\color{} {HgF\,aq} \;(無) \end{align}\] | \[\begin{align} &\rm\color {lightgray} {HgCl_2\,aq} \;(白)\\ &\rm\color{lightgray} {Hg_2Cl_2 \downarrow} \;(白) \end{align}\] | \[\rm \color {lightgray} {HgBr_2\downarrow} \;(白) \] | \[\begin{align} &\rm\color {orangered} {HgI_2 \downarrow} \;(赤橙)\;\\ &\rm\color {yellow} {Hg_2I_2 \downarrow} \;(黄)\; \end{align}\] |
ハロゲン化銀の錯イオン化
感光性をもつ.
| \[\rm NH_3 \] | \[\rm Na_2S_2O_3 \] | \[\rm KCN \] | |
|---|---|---|---|
| \[\rm \color{lightgray} {AgCl} \;(白) \] | \[\rm [Ag(NH_3)_2]^+ \;(無) \] | \[\rm [Ag(S_2O_3)_2]^{3-} \;(無) \] | \[\rm [Ag(CN)_2]^- \;(無) \] |
| \[\rm \color{khaki} {AgBr} \;(淡黄) \] | \[\rm [Ag(NH_3)_2]^+ \;(無) \] | \[\rm [Ag(S_2O_3)_2]^{3-} \;(無) \] | \[\rm [Ag(CN)_2]^- \;(無) \] |
| \[\rm \color{yellow} {AgI} \;(黄) \] | \[\rm \color{} {AgI\,aq} \;(無) \] | \[\rm [Ag(S_2O_3)_2]^{3-} \;(無) \] | \[\rm [Ag(CN)_2]^- \;(無) \] |
酸と金属
| \[\rm CO_3^{2-}\] | \[\rm SO_4^{2-}\] | \[\rm\color{yellow} {CrO_4^{2-}}\;(黄)\] | |
|---|---|---|---|
| \[\rm Li\] | \[\rm\color{lightgray} {Li_2CO_3}\;(白)\] | \[\begin{align} &\rm\color{lightgray} {Na_2SO_4(s)}\;(白)\\ &\rm\color{} {Li_2SO_4\,aq}\;(無) \end{align}\] | |
| \[\rm K\] | \[\begin{align} &\rm\color{lightgray} {K_2CO_3(s)}\;(白)\\ &{}^*\rm{K_2CO_3\,aq} \;(無)\end{align}\] | \[\begin{align} &\rm\color{lightgray} {K_2SO_4(s)}\;(白)\\ &\rm\color{} {K_2SO_4\,aq}\;(無) \end{align}\] | |
| \[\rm Ba\] | \[\rm\color{lightgray} {BaCO_3}\;(白)\] | \[{}^*\rm\underset {X線撮影の造影剤}{\underline{\color {lightgray}{BaSO_4}}}\;(白)\] | \[\rm\color{yellow} {BaCr_4}\;(黄)\] |
| \[\rm Sr\] | \[\rm\color{lightgray} {SrCO_3}\;(白)\] | \[{}^*\rm\color {lightgray}{SrSO_4} \;(白)\] | |
| \[\rm Ca\] | \[\rm \color {lightgray} {CaCO_3} \;(白) \] | \[{}^*\rm\color {lightgray}{CaSO_4} \;(白)\] | |
| \[\rm Na \] | \[\begin{align} &\rm\color{lightgray} {Na_2CO_3(s)}\;(白)\\ &{}^*\rm\color{} {Na_2CO_3\,aq}\;(無) \end{align}\] | \[\begin{align} &\rm\color{lightgray} {Na_2SO_4(s)}\;(白)\\ &\rm\color{} {Na_2SO_4\,aq}\;(無) \end{align}\] | |
| \[\rm Mg\] | \[\rm\color{lightgray} {MgCO_3}\;(白)\] | \[\begin{align} &\rm\color{lightgray} {MgSO_4(s)}\;(白)\\ &\rm\color{} {MgSO_4\,aq}\;(無) \end{align}\] | |
| \[\rm Al\] | \[\rm \color {lightgray} {Al_2(CO_3)_3} \;(白) \] | \[\begin{align} &\rm\color{lightgray} {Al_2(SO_4)_3(s)} \;(白)\\&\rm\color{} {Al_2(SO_4)_3\,aq} \;(無)\end{align}\] | |
| \[\rm Mn\] | \[\rm\color{khaki} {MnCO_3}\;(淡褐)\] | \[\begin{align} &\rm\color{pink} {MnSO_4(s)}\;(淡赤)\\ &\rm\color{pink} {MnSO_4\,aq}\;(淡赤) \end{align}\] | |
| \[\rm Zn\] | \[\rm\color{lightgray} {ZnCO_3}\;(白)\] | \[\begin{align} &\rm\color{lightgray} {ZnSO_4(s)}\;(白)\\ &\rm\color{} {ZnSO_4\,aq}\;(無) \end{align}\] | |
| \[\rm Cr\] | \[\rm\color{lightblue} {Cr_2(CO_3)_3}\;(淡青) \] | \[\begin{align} &\rm\color{purple} {Cr_2(SO_4)_3(s)} \;(赤紫)\\ &\rm\color{#00AE95} {Cr_2(SO_4)_3\,aq} \;(青緑)\end{align}\] | |
| \[\rm Fe\] | \[\rm\color{khaki} {FeCO_3}\;(ベージュ)\] | \[\begin{align} &\rm\color{lightgray} {FeSO_4(s)}\;(白)\\ &\rm\color{#61C1BE} {FeSO_4\cdot7H_2O(s)} \;(青緑)\\&\rm\color {lightgreen} {Fe^{2+}\,aq}\;(淡緑)\\\\ &\rm\color{lightgray} {Fe_2(SO_4)_3(s)} \;(灰白)\\&\rm\color {gold}{Fe^{3+}\,aq} \;(黄褐)\end{align}\] | |
| \[\rm Ni\] | \[\rm\color {lightgreen} {NiCO_3}\;(淡緑)\] | \[\begin{align} &\rm\color {yellowgreen} {NiSO_4(s)}\;(黄緑)\\ &\rm\color{#61C1BE} {NiSO_4\cdot6H_2O(s)} \;(青緑)\\ &\rm\color{green} {Ni^{2+}\,aq}\;(緑) \end{align}\] | |
| \[\rm Sn\] | \[\begin{align} &\rm\color{lightgray} {SnCO_3}\;(白)\\ &\rm\color{lightgray} {Sn(CO_3)_2}\;(白) \end{align}\] | \[\begin{align} &\rm\color {lightyellow} {SnSO_4(s)}\;(淡黄)\\ &\rm\color{} {Sn^{2+}\,aq}\;(無) \end{align}\] | |
| \[\rm Pb\] | \[\rm\color{lightgray} {PbCO_3}\;(灰白)\] | \[{}^*\rm\color {lightgray}{PbSO_4} \;(白)\] | \[\rm\color{yellow} {PbCr_4}\;(黄)\] |
| \[\rm Cu\] | \[\begin{align} &\rm\color{#61C1BE} {CuCO_3\cdot Cu(OH)_2}\;(青緑)\\ &\rm\color{#61C1BE} {2CuCO_3\cdot Cu(OH)_2}\;(青緑) \end{align}\] | \[\begin{align} &\rm\color{lightgray} {CuSO_4(s)}\;(白)\\ &\rm\color{blue} {CuSO_4\cdot 5H_2O(s)}\;(青)\\ &\rm\color{blue} {CuSO_4\,aq}\;(青) \end{align}\] | |
| \[\rm Hg\] | \[\rm\color{gold} {Hg_2CO_3}\;(黄褐)\] | \[\begin{align} &\rm\color {lightyellow} {Hg_2SO_4(s)}\;(淡黄)\\ &\rm\color {lightyellow} {HgSO_4(s)}\;(淡黄)\\ &水溶液色不明 \end{align}\] | |
| \[\rm Ag\] | \[\rm\color {lightgreen} {Ag_2CO_3}\;(淡黄緑)\] | \[\begin{align} &\rm\color{} {Ag_2SO_4(s)}\;(無)\\ &\rm\color{} {Ag_2SO_4\,aq}\;(無)\ \end{align}\] | \[\rm\color{darkred} {Ag_2Cr_4}\;(赤褐)\] |
| \[\rm Pt\] | – | – | |
| \[\rm Au\] | – | – | |
| \[\rm NH_3\] | \[\begin{align} &\rm\color{lightgray} {(NH_4)_2CO_3(s)} \;(白)\\ &{}^*\rm\color{} {(NH_4)_2CO_3\,aq} \;(無)\end{align}\] | \[\begin{align} &\rm\color{lightgray} {(NH_4)_2SO_3(s)} \;(白)\\&\rm\color{} {(NH_4)_2SO_3\,aq} \;(無)\end{align}\] |
塩として沈殿しない酸
| \[\begin{align} &\rm\color{orangered}{Cr_2O_7^{2-}}\;(赤橙)\quad\\ &\rm\color{violet}{MnO_4^{-}}\;(赤紫)\\ &\rm\color{darkgreen}{MnO_4^{2-}}\;(暗緑) \end{align}\] |
鉄イオン×シアニド錯イオン
| \[\rm K_4[Fe(CN)_6] \] | \[\rm K_3[Fe(CN)_6] \] | |
|---|---|---|
| \[\rm \color{aquamarine} {Fe^{2+}} \;(淡緑) \] | \[\rm \color{skyblue} {不定} \downarrow(青白) \] | \[\rm \color{darkblue} {KFe^{I\!I}Fe^{I\!I\!I}(CN)_6} \downarrow(濃青) \] |
| \[\rm \color{gold} {Fe^{3+}} \;(黄褐) \] | \[\rm \color{darkblue} {KFe^{I\!I}Fe^{I\!I\!I}(CN)_6} \downarrow(濃青) \] | \[\rm \color{brown} {不定} \;(褐) \] |
鉄イオン×チオシアン酸カリウム
| \[\begin{align} &\rm\color{gold}{Fe^{3+}}\;(黄褐) &&\xrightarrow{\rm KSCN\,aq} &&\rm\color{darkred}{[Fe(SCN)(H_2O)_5]^{2+}}\;(血赤)\quad \end{align}\] |
塩化コバルト紙
| \[\begin{align} &\rm\color{blue}{CoCl_2}\;(青) &&\xrightarrow{\rm H_2O} &&\rm\color{lightpink}{[Co(H_2O)_6]^{2+}}\;(淡紅)\quad \end{align}\] |
風解
| 風解 | 潮解 |
|---|---|
| \[\rm AlK(SO_4)_2\cdot12H_2O\quad(ミョウバン)\] | \[\rm K_2CO_3\] |
| \[\rm CaCl_2\] | |
| \[\rm Na_2CO_3\cdot 10H_2O\] | \[\rm NaOH\] |
| \[\rm MgCl_2\] | |
| \[\rm CuSO_4\cdot5H_2O\] | |
| \[\rm C_6H_8O_7\quad(クエン酸)\] | |
| \[\rm P_4O_{10},\;H_3PO_4\] |
合金
| 合金 | 成分 | 用例 |
|---|---|---|
| ジュラルミン | \[\rm Al\text{-}Cu \text{-}Mg\text{-}Mn\] | 航空機,鉄道車両,ノートPC |
| チタン合金 | \[\rm Ti\text{-}Al\text{-}V\] | 航空機,車体フレーム,人工骨・関節 |
| 鋼 | \[\rm Fe\text{-}C\] | 建築物,車体フレーム |
| ステンレス鋼 | \[\rm Fe\text{-}Cr \text{-}Ni\text{-}C\] | シンク,包丁,鉄道車両 |
| ニクロム | \[\rm Ni\text{-}Cr\] | 電熱器,ドライヤー |
| 青銅(ブロンズ) | \[\rm Cu\text{-}Sn\] | 美術工芸品,10円玉 |
| 黄銅(真鍮) | \[\rm Cu\text{-}Zn\] | 装飾品,金管楽器,5円玉 |
| 白銅 | \[\rm Cu\text{-}Ni\] | 100円玉 |
| 形状記憶合金 | \[\rm TiNi\] | メガネ,車体フレーム,温度センサー |
| 水素吸蔵合金 | \[\rm LaNi_5\] | ニッケル水素電池の負極 |
| 超伝導合金 | \[\rm Nb_3Sn\] | MRI |
| アモルファス合金 | \[\begin{align} &\rm Fe\text{-}Si\text{-}B\\ &\rm Fe\text{-}Cr\text{-}P \text{-}C\quad etc. \end{align}\] | 小型モーターギア,スポーツ用品 |
製法
ハーバーボッシュ法
| \[\begin{align} &\rm N_2+3H_2 \xrightarrow [\rm Fe_3O_4] {400\text{-}600\;{\rm[{}^\circ C]},\;200\text{-}1000\;{\rm[atm]}} 2NH_3 &&{\it\Delta}H=-92\;\rm[kJ] \end{align}\] |
オストワルト法
| \[\begin{align} &\begin{cases} \rm 4NH_3+5O_2 \xrightarrow[Pt]{800\;[{}^\circ C]} \color{brown}{4NO}\;(赤褐)+6H_2O\\\\ \rm \color{brown}{2NO}+O_2 \rightarrow 2NO_2\\\\ \rm 3NO_2+H_2O \rightarrow 2NO_3+NO \end{cases} &&\Rightarrow &&\rm NH_3+2O_2 \rightarrow HNO_3 +H_2O \end{align}\] |
接触法
アンモニアソーダ法(ソルベー法)
アンモニアの分解
| \[\rm NH_4\rightarrow N_2+H_2O\] |
ガラス
ソーダ石灰ガラス(一般的なガラス)
| \[\rm \underset{珪砂}{\underline{SiO_2}}+Na_2CO_3+CaCO_3 \xrightarrow{1000{}^\circ C} SiO_2\text{-}Na_2O\text{-}CaO\] |
水ガラス(珪酸ソーダ)
| \[\rm \underset{水ガラス}{\underline{Na_2O\cdot n\,SiO_2\cdot m\,H_2O\,(l)}} \xrightarrow{HCl}\underset{珪酸}{\underline{H_2SiO_3\,(gel)}} \xrightarrow{脱水}\underset{シリカゲル}{\underline{SiO_2\cdot k\,H_2O\,(s)}}\] |
消石灰・さらし粉・高度さらし粉
消石灰は,漆喰の主成分.
| \[\rm\underset{石灰水(消石灰)}{\underline{Ca(OH)_2}}+2Cl_2 \rightarrow\underset{さらし粉}{\underline{CaCl(ClO)\cdot H_2O}}+Cl_2 \rightarrow\underset{高度さらし粉}{\underline{Ca(ClO)_2}}+2HCl\] |
塩素酸カリウム+二酸化マンガン
| \[\rm\underset{塩素酸カリウム}{\underline{2KClO_3}} \xrightarrow{MnO_2}2KCl+3O_2\] |
石膏・焼き石膏
| \[\rm \underset{石膏}{\underline{CaSO_4\cdot2H_2O}} \xrightarrow{\Delta}\underset{焼き石膏}{\underline{CaSO_4\cdot\frac{1}{2}H_2O}}\] |
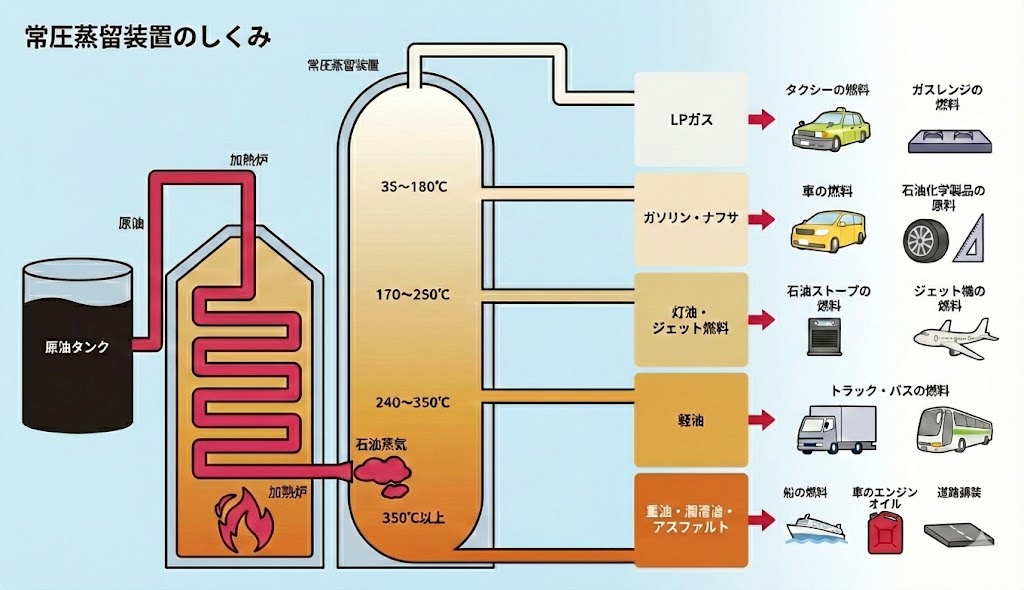
石油
コロイド
疎水コロイドを速く凝析させる場合,コロイドと逆符号でイオンあたりの価数の差が大きいものを選ぶ.
電池
イオン化傾向
| \[\begin{align} &語呂「理科馬鹿な,ま,甘ーくて,にすんな,ひどすぎ,借金」&&\\\\ &\begin{aligned} &冷水&&\rm Li>K>Ba>Ca>Na\\\\ &熱水&&\rm Mg\\\\ &水蒸気&&\rm Al>Mn>Zn>Cr>Fe\\\\ &希酸&&\rm Ni>Sn>Pb\\\\ &高酸化力の酸\qquad&&\rm H_2>Cu>Hg>Ag\\\\ &王水&&\rm Pt>Au \end{aligned} \end{align}\] |
マンガン乾電池
アルカリマンガン乾電池
空気電池
リチウム電池
鉛蓄電池
| \[\begin{align} &\begin{cases}+:&\rm PbO_2+SO_4^{2-}+4H^++2e^-\rightarrow PbSO_4+2H_2O\\\\ -:&\rm Pb+SO_4^{2-}\rightarrow PbSO_4+2e^-\end{cases}\\\\ &\Rightarrow\quad \rm Pb+PbO_2+2H_2SO_4\rightarrow 2PbSO_4+2H_2O \end{align}\] |